OMS e IARC classificam aspartame como possivelmente carcinogênico
 A avaliação dos impactos na saúde do aspartame foi divulgada pela Organização Mundial da Saúde (OMS), em análise realizada pelo Comitê Conjunto de Especialistas em Aditivos Alimentares da Organização para Agricultura e Alimentação (Joint FAO/WHO Expert Committee on Food Additives – JECFA) e pela Agência Internacional de Pesquisa sobre o Câncer (IARC). Citando evidências limitadas de carcinogenicidade em humanos, a IARC classificou o aspartame como possivelmente carcinogênico para humanos (IARC Grupo 2B) e o JECFA reafirmou ser aceitável a ingestão diária de 40 mg/kg de peso corporal.
A avaliação dos impactos na saúde do aspartame foi divulgada pela Organização Mundial da Saúde (OMS), em análise realizada pelo Comitê Conjunto de Especialistas em Aditivos Alimentares da Organização para Agricultura e Alimentação (Joint FAO/WHO Expert Committee on Food Additives – JECFA) e pela Agência Internacional de Pesquisa sobre o Câncer (IARC). Citando evidências limitadas de carcinogenicidade em humanos, a IARC classificou o aspartame como possivelmente carcinogênico para humanos (IARC Grupo 2B) e o JECFA reafirmou ser aceitável a ingestão diária de 40 mg/kg de peso corporal.



 Pesquisa publicada no Blood Advances destaca a potencial associação entre índice de massa corporal (IMC) elevado e resultados inferiores no tratamento para leucemia linfoblástica aguda (LLA) em adolescentes e adultos jovens. O estudo lança luz sobre o impacto do peso nas toxicidades e nos resultados terapêuticos, em análise que identificou piores desfechos clínicos entre indivíduos com obesidade ou sobrepeso, com menores taxas de sobrevida.
Pesquisa publicada no Blood Advances destaca a potencial associação entre índice de massa corporal (IMC) elevado e resultados inferiores no tratamento para leucemia linfoblástica aguda (LLA) em adolescentes e adultos jovens. O estudo lança luz sobre o impacto do peso nas toxicidades e nos resultados terapêuticos, em análise que identificou piores desfechos clínicos entre indivíduos com obesidade ou sobrepeso, com menores taxas de sobrevida.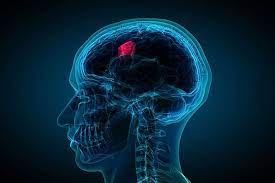 Craniofaringiomas são tumores cerebrais primários do eixo hipófise-hipotálamo e podem causar sequelas clinicamente significativas. Em artigo na New England Journal of Medicine, Brastianos et al. mostram que em pequeno estudo de braço único, 15 de 16 pacientes tiveram uma resposta parcial ou melhor à inibição BRAF-MEK. “Todos os pacientes que completaram um ou mais ciclos da terapia responderam ao tratamento, que é a maior taxa de resposta até o momento de qualquer terapia médica para tumores cerebrais”, disse a primeira autora, Priscilla Brastianos, do Mass General Cancer Center.
Craniofaringiomas são tumores cerebrais primários do eixo hipófise-hipotálamo e podem causar sequelas clinicamente significativas. Em artigo na New England Journal of Medicine, Brastianos et al. mostram que em pequeno estudo de braço único, 15 de 16 pacientes tiveram uma resposta parcial ou melhor à inibição BRAF-MEK. “Todos os pacientes que completaram um ou mais ciclos da terapia responderam ao tratamento, que é a maior taxa de resposta até o momento de qualquer terapia médica para tumores cerebrais”, disse a primeira autora, Priscilla Brastianos, do Mass General Cancer Center. Estudo de Walker et al. publicado no BMC confirmou a associação do tratamento quimioterápico com ganho de peso e possíveis alterações antropométricas deletérias, sugerindo que alterações da flora bacteriana podem contribuir para esses fenômenos através da indução da inflamação sistêmica.
Estudo de Walker et al. publicado no BMC confirmou a associação do tratamento quimioterápico com ganho de peso e possíveis alterações antropométricas deletérias, sugerindo que alterações da flora bacteriana podem contribuir para esses fenômenos através da indução da inflamação sistêmica. Estudo que analisou o valor terapêutico das indicações novas e suplementares de medicamentos aprovados nos Estados Unidos e na Europa mostrou que menos da metade das primeiras indicações aprovadas nos EUA e na Europa foram classificadas como de alto valor terapêutico, percentual ainda menor para indicações suplementares.
Estudo que analisou o valor terapêutico das indicações novas e suplementares de medicamentos aprovados nos Estados Unidos e na Europa mostrou que menos da metade das primeiras indicações aprovadas nos EUA e na Europa foram classificadas como de alto valor terapêutico, percentual ainda menor para indicações suplementares.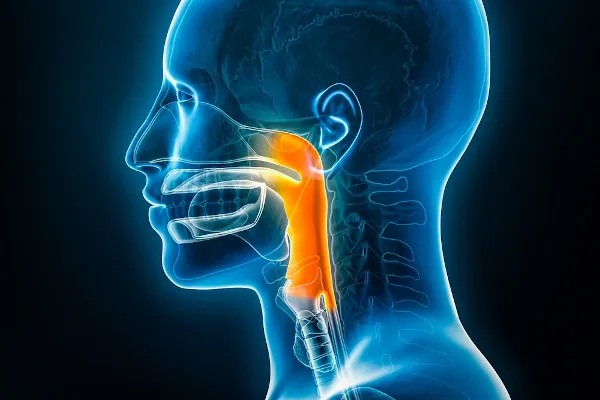 Estudo de pesquisadores da Cancer Research UK avaliou se a radioterapia de intensidade modulada otimizada para disfagia (DO-IMRT) reduziu a dose de radiação na disfagia e nas estruturas relacionadas à aspiração e se melhorou a função de deglutição em comparação com a radioterapia de intensidade modulada (IMRT) padrão. Os resultados foram publicados online no Lancet Oncology e sugerem benefício da DO-IMRT para pacientes que recebem radioterapia para câncer de faringe.
Estudo de pesquisadores da Cancer Research UK avaliou se a radioterapia de intensidade modulada otimizada para disfagia (DO-IMRT) reduziu a dose de radiação na disfagia e nas estruturas relacionadas à aspiração e se melhorou a função de deglutição em comparação com a radioterapia de intensidade modulada (IMRT) padrão. Os resultados foram publicados online no Lancet Oncology e sugerem benefício da DO-IMRT para pacientes que recebem radioterapia para câncer de faringe. Publicado no JCO Global Oncology, artigo de revisão realizado por pesquisadores do ICESP e da FMUSP traça um panorama do carcinoma hepatocelular no Brasil, analisando o contexto geral de saúde e as particularidades regionais para contribuir com a implementação de medidas que possam melhorar os resultados dos pacientes no país. Leonardo Fonseca (na foto, à direita) é o primeiro autor do trabalho, que tem o professor Flair Carrilho como autor sênior.
Publicado no JCO Global Oncology, artigo de revisão realizado por pesquisadores do ICESP e da FMUSP traça um panorama do carcinoma hepatocelular no Brasil, analisando o contexto geral de saúde e as particularidades regionais para contribuir com a implementação de medidas que possam melhorar os resultados dos pacientes no país. Leonardo Fonseca (na foto, à direita) é o primeiro autor do trabalho, que tem o professor Flair Carrilho como autor sênior. Vários estudos demonstraram efeitos nocivos do uso de cigarros eletrônicos, mas pesquisadores iranianos avaliaram pela primeira vez os efeitos dos chamados e-cigarettes na saúde da próstata, demonstrando que a toxicidade é comparável à do tabagismo convencional.
Vários estudos demonstraram efeitos nocivos do uso de cigarros eletrônicos, mas pesquisadores iranianos avaliaram pela primeira vez os efeitos dos chamados e-cigarettes na saúde da próstata, demonstrando que a toxicidade é comparável à do tabagismo convencional. A identificação de fatores de risco para o câncer colorretal de início precoce (EOCRC) pode ajudar a reverter sua incidência crescente. Estudo de Imperiale et al no Cancer Prevention Research buscou identificar fatores de risco para EOCRC, com achados que podem ser usados para identificar quem pode se beneficiar do rastreamento para câncer colorretal antes dos 45 ou 50 anos.
A identificação de fatores de risco para o câncer colorretal de início precoce (EOCRC) pode ajudar a reverter sua incidência crescente. Estudo de Imperiale et al no Cancer Prevention Research buscou identificar fatores de risco para EOCRC, com achados que podem ser usados para identificar quem pode se beneficiar do rastreamento para câncer colorretal antes dos 45 ou 50 anos. Os inibidores de tirosina quinase de Bruton (BTKis) são o tratamento padrão para múltiplas malignidades de células B. Artigo de Philip A. Thompson e Constantine S. Tam publicado na Blood sintetiza os principais dados pré-clínicos e clínicos existentes para pirtobrutinib, um BTKi não covalente que obteve recente aprovação acelerada da Food and Drug Administration (FDA) para o tratamento de pacientes com Linfoma de Células do Manto (LCM).
Os inibidores de tirosina quinase de Bruton (BTKis) são o tratamento padrão para múltiplas malignidades de células B. Artigo de Philip A. Thompson e Constantine S. Tam publicado na Blood sintetiza os principais dados pré-clínicos e clínicos existentes para pirtobrutinib, um BTKi não covalente que obteve recente aprovação acelerada da Food and Drug Administration (FDA) para o tratamento de pacientes com Linfoma de Células do Manto (LCM).
