Em mais um tópico da coluna ‘Drops de Genômica’, o oncologista Andre Murad discute os resultados de estudo publicado no JAMA Oncology que avaliou a baixa prevalência de HER2 IHQ 3+ entre diferentes tipos de tumor em um cenário de mundo real. Confira.
Por André Marcio Murad*
Estudo publicado recentemente no JAMA Oncology sugere que a incidência de positividade para HER2 é baixa em todos os tipos de tumor. Pesquisadores testaram mais de 65 mil pacientes com mais de 30 tipos de tumores sólidos e constataram que a taxa de positividade para HER2 foi de cerca de 3%.
O estudo incluiu 65.075 pacientes com tumores sólidos malignos submetidos à imuno-histoquímica (IHQ) para HER2 utilizando o ensaio Ventana PATHWAY anti-HER2/neu. O teste foi realizado pela Caris Life Sciences após a aprovação acelerada do trastuzumabe deruxtecano-nxki para o tratamento de adultos com tumores sólidos HER2-positivos irressecáveis ou metastáticos que receberam tratamento sistêmico e sem opções alternativas de tratamento (indicação agnóstica).
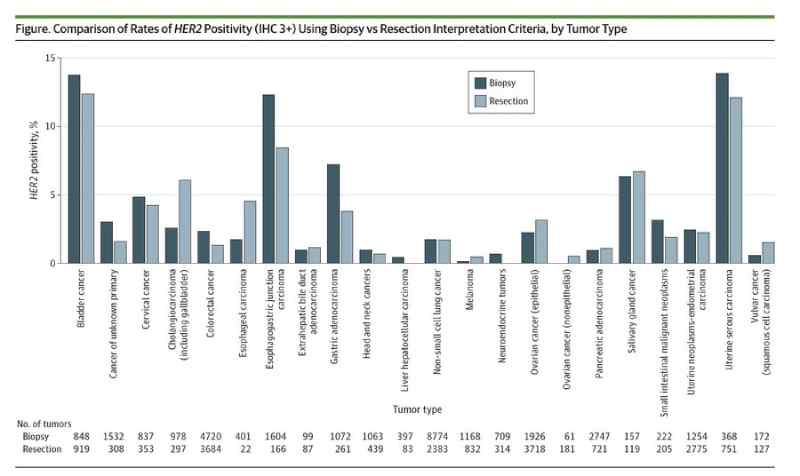
Os tumores foram considerados HER2 positivos se a pontuação IHQ fosse 3+. Casos positivos para IHQ 2+/hibridização in situ para HER2 foram excluídos da análise. Para outros tipos de câncer, além do câncer de mama, o status do HER2 foi determinado com base em critérios de interpretação de biópsia gástrica ou ressecção, dependendo do procedimento realizado.
As maiores taxas de positividade para HER2 foram observadas em câncer de bexiga (13,9%), carcinoma seroso uterino (13,6%), câncer da junção esofagogástrica (12,1%), carcinoma de mama (7,8%) e adenocarcinoma gástrico (6,6%). As taxas de positividade para HER2 foram baixas entre pacientes com câncer renal (0,1%), adenocarcinoma de próstata (0,2%), melanoma (0,3%), câncer de ovário não epitelial (0,4%) e carcinoma hepatocelular (0,4%). Não houve casos de positividade para HER2 entre pacientes com gliomas, sarcomas, câncer de pulmão de pequenas células, tumores estromais gastrointestinais, carcinoma de tireoide, sarcoma uterino, carcinoma tímico e carcinoma de células de Merkel.
Do ponto de vista da necessidade médica e do custo, este estudo propõe que o teste IHC de HER2 inicial possa não ser necessário para todos os tipos de tumores, especialmente aqueles que raramente são positivos. O perfil genômico abrangente poderia ser usado como um teste de triagem, por meio do qual a IHC de HER2 seria realizada em tumores com amplificação do número de cópias de ERBB2 e/ou superexpressão do gene do RNA mensageiro de ERBB2. Essa abordagem simplificada poderia otimizar os fluxos de trabalho laboratoriais e reduzir testes desnecessários.
*André Murad é diretor científico do Grupo Brasileiro de Oncologia de Precisão (GBOP), diretor clínico da Personal - Oncologia de Precisão e Personalizada, professor adjunto coordenador da Disciplina de Oncologia da Faculdade de Medicina da UFMG, e oncologista e oncogeneticista da Clínica OncoLavras





