No carcinoma espinocelular cutâneo (CEC) de alto risco, o tratamento adjuvante com cemiplimabe prolongou a sobrevida livre de doença (SLD) e reduziu o risco de recorrência na comparação com placebo, como demonstram resultados do estudo de fase 3 C-POST apresentados no ASCO 2025 e publicados simultaneamente na New England Journal of Medicine (NEJM)1. Cemiplimabe adjuvante mostrou benefício sem precedentes nessa população de pacientes, reduzindo em 68% o risco de recidiva da doença ou morte; em 24 meses a SLD foi de 87,1% no grupo tratado com cemiplimabe adjuvante contra 64,1% no grupo controle.
O câncer de pele não melanoma é a neoplasia mais frequente no Brasil, sendo o carcinoma espinocelular (CEC) e o carcinoma basocelular (CBC) os subtipos mais presentes. De acordo com o Instituto Nacional do Câncer (INCA)2, 704 mil novos casos são estimados no país em 2025. Globalmente, o CEC cutâneo é a segunda forma mais comum de câncer de pele, com aproximadamente 2,4 milhões de novos casos e 56.000 mortes em 2019. De 1990 a 2019, a incidência global aumentou em mais de 200%, como revela análise que envolveu mais de 204 países e territórios3.
Cemiplimabe (Libtayo®) é um anticorpo que bloqueia a proteína PD-1, aprovado como tratamento padrão para pacientes com CEC avançado, associado a taxas de resposta em cerca de 50% dos pacientes com doença metastática/irressecável, com controle duradouro e melhora da qualidade de vida4,5. Os resultados encorajadores da imunoterapia com cemiplimabe no cenário do CEC avançado também embasaram estudos com cemiplimabe no contexto neoadjuvante. Administrado na dose de 350 mg a cada 3 semanas por até quatro doses antes da cirurgia com intenção curativa, cemiplimabe neoadjuvante foi associado à resposta patológica completa em 51% dos pacientes com CEC cutâneo em estágio II, III ou IV (M0). Na avaliação da resposta baseada em imagem, de acordo com os critérios RECIST (v1.1), 68% dos pacientes alcançaram resposta objetiva com cemiplimabe neoadjuvante6.
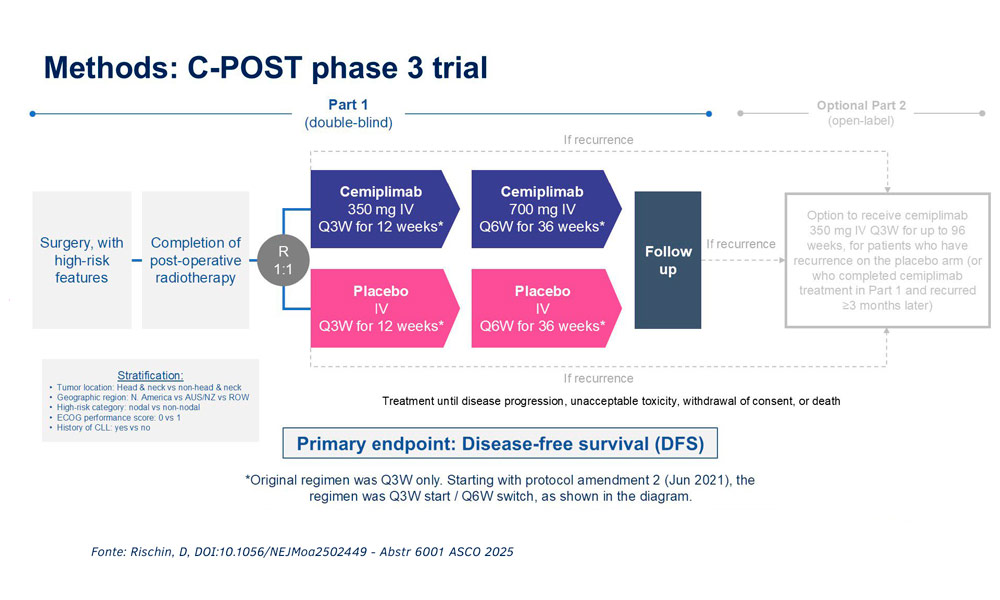
Apesar dos avanços, não há tratamento sistêmico aprovado para pacientes com CEC com alto risco de recorrência locorregional ou à distância, após cirurgia com intenção curativa e radioterapia adjuvante. C-POST é um estudo randomizado, duplo-cego, multicêntrico, de fase 3, que busca avaliar cemiplimabe nessa população de pacientes.
Neste estudo global (NCT03969004), foram inscritos pacientes adultos (≥ 18 anos) com CEC local e/ou regional, após cirurgia e radioterapia pós-operatória, considerados de alto risco de recorrência de acordo com critérios ganglionares (extensão extracapsular com o maior linfonodo ≥ 2 cm ou ≥ 3 linfonodos envolvidos) e/ou não ganglionares (metástases em trânsito, lesão T4, invasão perineural ou tumor localmente recorrente com ≥ 1 característica de risco adicional).
Os pacientes foram randomizados na proporção de 1:1 para receber cemiplimabe adjuvante (350 mg) ou placebo, administrado por via intravenosa a cada 3 semanas durante 12 semanas, seguido de um aumento da dose para 700 mg, administrado a cada 6 semanas, por até 36 semanas (≤48 semanas no total). O desfecho primário foi a sobrevida livre de doença. Os desfechos secundários incluíram ausência de recorrência locorregional, ausência de recorrência à distância e segurança.
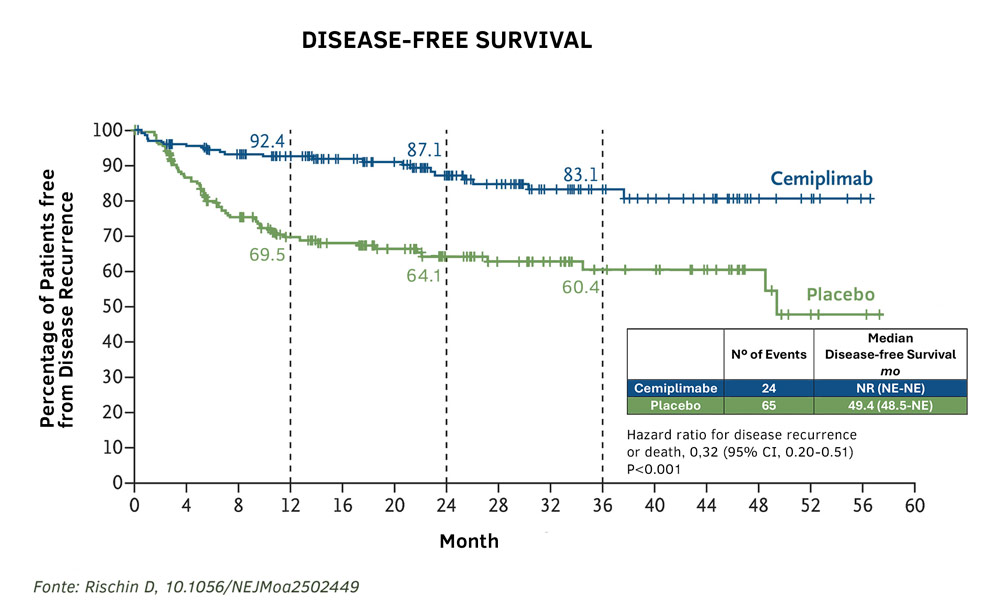
Um total de 415 pacientes foram randomizados para cemiplimabe (n= 209) ou placebo (n=206). O acompanhamento mediano foi de 24 meses. Os resultados apresentados no ASCO 2025 e publicados simultaneamente na NEJM por Rischin et al. mostram que cemiplimabe atingiu o desfecho primário e foi superior ao placebo em relação à sobrevida livre de doença (24 vs. 65 eventos; razão de risco (HR) para recorrência da doença ou óbito, 0,32; intervalo de confiança [IC] de 95%, 0,20 a 0,51; P < 0,001). A sobrevida livre de doença estimada em 24 meses foi de 87,1% (IC de 95%, 80,3 a 91,6) com cemiplimabe e de 64,1% (IC de 95%, 55,9 a 71,1) com placebo (veja gráfico).
“Cemiplimabe adjuvante mostrou ganho bastante significativo de SLD nessa população de pacientes com CEC de alto risco, com hazard ratio de 0,32, e em três anos o ganho absoluto foi de 23%”, analisa Gustavo Schvartsman, oncologista do Hospital Israelita Albert Einstein. “A magnitude do benefício deve levar à aprovação de cemiplimabe no cenário adjuvante pelas principais autoridades reguladoras”.
Cemiplimabe também cumpriu os principais desfechos secundários, reduzindo significativamente o risco de recorrência locorregional (9 eventos vs. 40 com placebo; razão de risco, 0,20; IC de 9%, 0,09 a 0,40) e de recorrência à distância (10 vs. 26 eventos; razão de risco, 0,35; IC de 95%, 0,17 a 0,72).
Nesta análise primária, o estudo C-POST mostrou que a recorrência locorregional foi mais frequente que a recorrência à distância, achado consistente com os resultados do estudo POST/TROG 05.01.O risco de recorrência locorregional foi 80% menor com a terapia adjuvante com cemiplimabe versus placebo, enquanto o risco de recorrência à distância foi 65% menor com cemiplimabe.
Em relação ao perfil de segurança e tolerabilidade, eventos adversos emergentes do tratamento (EAETs) de grau ≥ 3 ocorreram em 23,9% e 14,2%, e descontinuações por EAETs ocorreram em 9,8% e 1,5% dos pacientes que receberam cemiplimabe e placebo, respectivamente. Em análises exploratórias, os benefícios de SLD foram observados em pacientes com PD-L1 tumoral ≥1% (HR 0,28; IC 95% 0,15–0,52; n=309) e <1% (HR 0,32; 0,12–0,86; n=85).
Em conclusão, nesta análise primária do ensaio clínico C-POST, o tratamento adjuvante com cemiplimabe prolongou a sobrevida livre de doença em pacientes com alto risco de recorrência de carcinoma espinocelular cutâneo. Cemiplimabe é a primeira terapia sistêmica a demonstrar resultados amplamente positivos como terapia adjuvante para CEC de alto risco, com redução clínica e estatisticamente significativa na recorrência da doença e perfil de segurança aceitável neste cenário.
Dados do estudo de Fase 3 (KEYNOTE-630)7 também apresentados no ASCO 2025 mostraram que o anti PD-1 pembrolizumabe (Keytruda®) falhou como estratégia adjuvante nessa população de pacientes. Dados de análise pré-planejada mostraram que pembrolizumabe não ultrapassou o limite de significância estatística na sobrevida livre de recidiva, desfecho primário do estudo. O desfecho secundário principal do estudo, sobrevida global, não foi testado formalmente, mas os resultados da análise pré-planejada não favoreceram o braço de intervenção com pembrolizumabe na comparação com placebo no CEC de alto risco. Diante desses resultados, o estudo KEYNOTE-630 foi descontinuado por recomendação do Comitê Independente de Monitoramento de Dados.
“Embora a cirurgia seja curativa para a maioria das pessoas que vivem com carcinoma espinocelular cutâneo, muitas correm risco maior de recorrência, que pode levar à morte ou desfiguração”, disse Danny Rischin, líder de Pesquisa em Câncer de Cabeça e Pescoço e CEC cutâneo do Peter MacCallum Cancer Centre, principal investigador do estudo C-POST. “Na primeira análise interina pré-especificada, cemiplimabe atingiu um nível notavelmente alto na melhoria da sobrevida livre de doença em pacientes com carcinoma espinocelular cutâneo de alto risco. Sem opções atualmente aprovadas no ambiente adjuvante, esses resultados demonstram que cemiplimabe pode representar grande avanço ao retardar a recorrência nesses pacientes vulneráveis”, destacou.
VÍDEO:
ASCO 2025: cemiplimabe é a primeira terapia sistêmica a reduzir recorrência do CEC de alto risco
Cemiplimabe adjuvante mostrou benefício sem precedentes no tratamento do carcinoma espinocelular cutâneo (CEC) de alto risco, reduzindo em 68% o risco de recidiva da doença ou morte. Em 24 meses, a SLD foi de 87,1% no grupo tratado com cemiplimabe adjuvante contra 64,1% no grupo controle. Gustavo Schvartsman, oncologista do Hospital Israelita Albert Einstein, fala em vídeo sobre o estudo C-POST que foi um dos destaques no Congresso Anual da Sociedade Americana de Oncologia Clínica (ASCO) de 2025. Assista:
- Rischin D, Porceddu S, Day F, Brungs D, Christie H, Jackson J, Stein B. Adjuvant Cemiplimab or Placebo in High-Risk Cutaneous Squamous-Cell Carcinoma. DOI: 10.1056/NEJMoa2502449. https://www.nejm.org/doi/full/10.1056/NEJMoa2502449
- Santos M de O, Lima FC da S de, Martins LFL, Oliveira JFP, Almeida LM de, Cancela M de C. Estimativa de Incidência de Câncer no Brasil, 2023-2025. Rev. Bras. Cancerol. [Internet]. 6º de fevereiro de 2023 [citado 2 de junho de 2025];69(1):e-213700. Disponível em: https://rbc.inca.gov.br/index.php/revista/article/view/3700
- Guo A, Liu X, Li H, Cheng W, Song Y, Raijmakers N. The global, regional, national burden of cutaneous squamous cell carcinoma (1990–2019) and predictions to 2035. Eur J Cancer Care (Engl) 2023; 2023(1). https://onlinelibrary.wiley.com/doi/10.1155/2023/5484597
- Hughes BGM, Guminski A, Bowyer S, et al. A phase 2 open-label study of cemiplimab in patients with advanced cutaneous squamous cell carcinoma (EMPOWER-CSCC-1): final long-term analysis of groups 1, 2, and 3, and primary analysis of fixed-dose treatment group 6. J Am Acad Dermatol 2025;92:68-77. https://www.jaad.org/article/S0190-9622(24)02770-1/abstract
- Migden MR, Rischin D, Schmults CD, et al. PD-1 blockade with cemiplimab in advanced cutaneous squamous-cell carcinoma. N Engl J Med 2018;379:341-351. https://www.nejm.org/doi/full/10.1056/NEJMoa1805131
- N.D. Gross, D.M. Miller, N.I. Khushalani, V. Divi, E.S. Ruiz, E.J. Lipson, et al. Neoadjuvant cemiplimab for stage II to IV cutaneous squamous-cell carcinoma. N. Engl. J. Med., 387 (17) (2022), pp. 1557-1568. https://www.nejm.org/doi/full/10.1056/NEJMoa1805131
- Shlomo A. Koyfman et al. Phase 3 randomized trial (KEYNOTE-630) of adjuvant pembrolizumab (pembro) versus placebo (pbo) for high-risk locally advanced cutaneous squamous cell carcinoma (LA cSCC) following surgery and radiation (RT).. JCO 43, 6000-6000(2025). DOI:10.1200/JCO.2025.43.16_suppl.6000. https://ascopubs.org/doi/10.1200/JCO.2025.43.16_suppl.6000