 Thomas Martin (foto), da Universidade da California, apresenta no ASH 2022 análise de subgrupo de estudo de Fase 3 (IKEMA) que avaliou isatuximabe associado a carfilzomibe e dexametasona (isa-Kd) na recidiva precoce ou tardia de pacientes com mieloma múltiplo recidivado e/ou refratário. Os resultados mostram que a adição de Isa a Kd melhorou a sobrevida livre de progressão e a profundidade de resposta, tanto na recidiva precoce quanto na recidiva tardia, com perfil de segurança gerenciável.
Thomas Martin (foto), da Universidade da California, apresenta no ASH 2022 análise de subgrupo de estudo de Fase 3 (IKEMA) que avaliou isatuximabe associado a carfilzomibe e dexametasona (isa-Kd) na recidiva precoce ou tardia de pacientes com mieloma múltiplo recidivado e/ou refratário. Os resultados mostram que a adição de Isa a Kd melhorou a sobrevida livre de progressão e a profundidade de resposta, tanto na recidiva precoce quanto na recidiva tardia, com perfil de segurança gerenciável.
Dados já conhecidos demonstram que a combinação de Isa-Kd melhora significativamente a sobrevida livre de progressão em comparação com Kd em pacientes com MM recidivado (mediana de SLP de 35,7 vs. 19,2 meses; razão de risco [HR] 0,58; 95,4% CI, 0,42–0,79), promovendo aumento clinicamente significativo de negatividade da doença residual mínima (MRD-) (33,5% vs. 15,4%) e taxas de resposta completa (CR) (44,1% vs 28,5%) na população com intenção de tratar. Agora, esta análise de subgrupo atualiza dados de eficácia e segurança de Isa-Kd versus Kd comparando pacientes com MM que tiveram recaída precoce versus tardia.
Foram elegíveis pacientes com 1–3 linhas anteriores de tratamento, randomizados 3:2 para receber Isa-Kd (n=179) ou Kd (n=123). O tratamento foi administrado até a progressão da doença ou toxicidade inaceitável. Esses dados de longo prazo, com acompanhamento mediano de 44 meses, são da análise final pré-especificada de sobrevida livre de progressão (SLP) do ensaio IKEMA. Endpoints secundários incluíram resposta completa (CR), negatividade de doença residual mínima (MRD-) e segurança.
A recidiva precoce foi definida como a recidiva <12 meses desde o início da linha de tratamento (LOT) mais recente para pacientes com ≥2 LOT anteriores, <18 meses para pacientes com 1 LOT anterior e <12 meses pós transplante autólogo de células-tronco (ASCT). A recidiva tardia foi definida como a recidiva ≥12 meses desde o início do LOT mais recente para aqueles com ≥2 LOT anteriores e ≥18 meses para pacientes com 1 LOT anterior.
Resultados
A análise apresentada no ASH 2022 revelou 107 pacientes com recidiva precoce (61/179 [34,1%] no braço Isa-Kd e 46/123 [37,4%] no braço Kd, além de 176 pacientes com recidiva tardia (104 [58,1%] no braço Isa-Kd e 72 [58,5%] no braço Kd.
Entre os pacientes com recidiva precoce, o braço Isa-Kd teve maior proporção de pacientes com insuficiência renal (31,0% vs 15,4%) e menor incidência de pacientes com ISS Estágio I (31,1% vs. 54,3%) em comparação com o braço Kd. O número mediano de LOT anterior foi 2 para ambos os braços de tratamento em pacientes com recidiva precoce e no braço Kd de recidiva tardia. No braço Isa-Kd de recidiva tardia, os autores descrevem a mediana de 1 LOT anterior (55,8% tiveram 1 LOT anterior com Isa-Kd vs 48,6% pacientes com Kd). Na recaída tardia, mais pacientes tiveram anormalidade cromossômica 1q21+ com Isa-Kd (44,2%) vs Kd (33,3%).
No corte de dados, a mediana de SLP foi mais longa para pacientes tratados com Isa-Kd vs Kd em recidiva precoce (24,7 vs. 17,2 meses; HR 0,662 [IC 95,4%, 0,404–1,087]) e também entre os que receberam Isa-Kd na recidiva tardia (42,7 vs. 21,9 meses; HR, 0,542 [IC 95,4%, 0,353– 0,833]) (Figuras 1 e 2). As taxas de resposta global com Isa-Kd versus Kd foram 82,0% vs. 82,6% em pacientes com recidiva precoce e 90,4% vs. 86,1% em pacientes com recidiva tardia, respectivamente.
Mais pacientes obtiveram resposta parcial muito boa ou melhor com o regime contendo isatuximabe (recidiva precoce: 67,2% vs. 52,2%; recidiva tardia: 76,0% vs. 58,3%), MRD- (recidiva precoce: 24,6% vs. 15,2%; recidiva tardia: 37,5% vs. 16,7%) e taxas de MRD-CR (recidiva precoce: 18,0% vs. 10,9%; recidiva tardia: 30,8% vs. 13,9%) com Isa-Kd vs. Kd, respectivamente.
A análise de segurança revela que eventos adversos graves (Grau ≥ 3) emergentes do tratamento (TEAEs) foram semelhantes em ambos os braços de análise em pacientes com recidiva inicial, mas foram maiores no braço Isa-Kd em pacientes com recidiva tardia. No entanto, as taxas de TEAEs levando à descontinuação definitiva ou morte foram semelhantes em ambos os braços, independentemente de recidiva precoce ou tardia.
TEAEs de todos os graus relatados com mais frequência com Isa-Kd (diferença ≥10% vs. Kd) incluíram reações à infusão na recidiva precoce (41,0% vs. 6,5%) e na recidiva tardia (50,0% vs. 1,4%), infecção do trato respiratório superior (38,2% vs. 26,8%), fadiga (32,4% vs. 19,7%), dispneia (36,3% vs. 22,5%), bronquite (30,4% vs. 12,7%), tosse (23,5% vs. 11,3%) e gastroenterite (14,7% vs. 4,2%) em pacientes com recidiva tardia.
Entre as anormalidades laboratoriais hematológicas relatadas com mais frequência (≥5%) no braço Isa-Kd, Martin e colegas descrevem anemia de Grau 3 (42,6% vs. 30,4%), neutropenia de Grau 3 (18,0% vs. 4,3%) e trombocitopenia de Grau 3 e 4 (21,3 % vs. 15,2% e 18,0% vs 13,0%) em pacientes com recaída precoce e neutropenia de Grau 3 (13,7% vs. 8,5%) em pacientes com recidiva tardia com Isa-Kd vs. Kd, respectivamente.
Em conclusão, a adição de Isa a Kd melhorou a SLP e a profundidade da resposta, tanto na recidiva precoce quanto na recidiva tardia, consistente com o benefício observado na população geral do estudo IKEMA, com perfil de segurança administrável. “Esses resultados apoiam Isa-Kd como padrão de tratamento em pacientes com MM recidivado e/ou refratário, independentemente da recidiva precoce ou tardia”, destacam os autores. 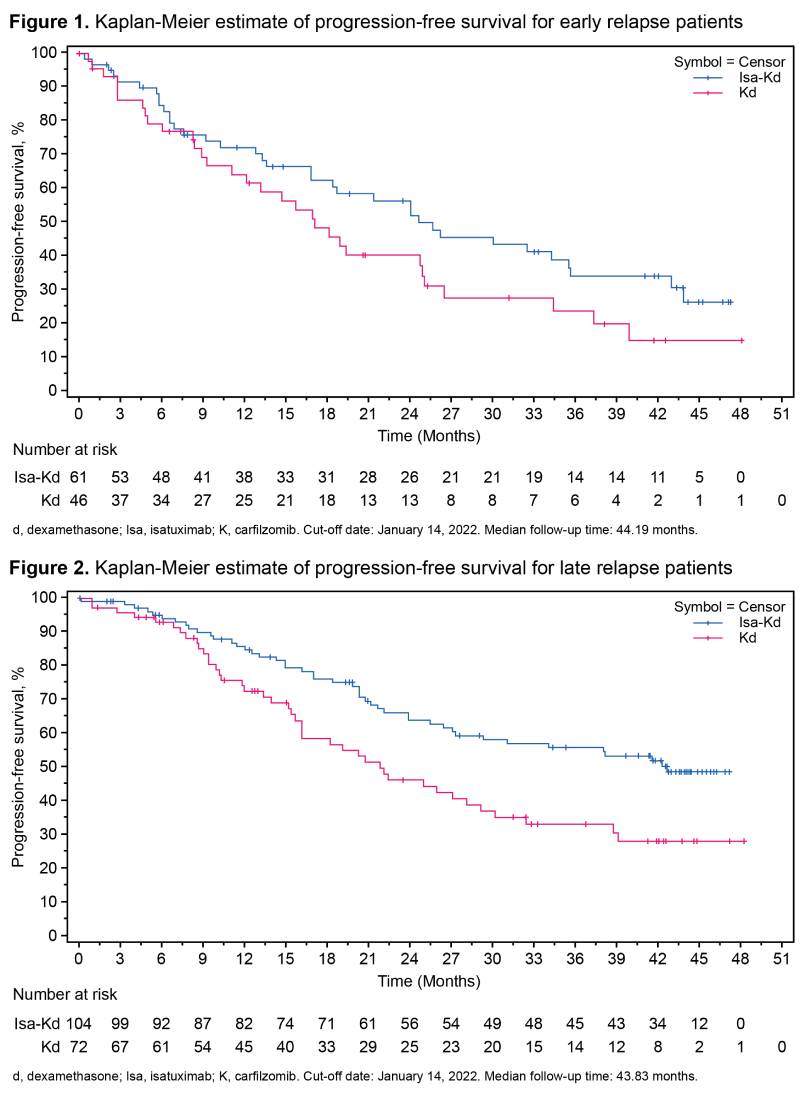
Referência: 753 Isatuximab Plus Carfilzomib and Dexamethasone in Patients with Early Versus Late Relapsed Multiple Myeloma: Ikema Subgroup Analysis
Program: Oral and Poster Abstracts
Type: Oral
Session: 652. Multiple Myeloma and Plasma Cell Dyscrasias: Clinical and Epidemiological: Therapeutic Impact in Multiple Myeloma
Monday, December 12, 2022: 11:00 AM
Thomas Martin, MD et al








