 Laercio Gomes Lourenço (foto), chefe do Grupo de Esôfago, Estômago, Duodeno e Intestino Delgado do Departamento de Cirurgia da Universidade Federal de São Paulo (UNIFESP) e presidente da Associação Brasileira de Câncer Gástrico, discute a videolaparoscopia no GIST gástrico, ressaltando sua indicação, as vantagens e os riscos desse procedimento.
Laercio Gomes Lourenço (foto), chefe do Grupo de Esôfago, Estômago, Duodeno e Intestino Delgado do Departamento de Cirurgia da Universidade Federal de São Paulo (UNIFESP) e presidente da Associação Brasileira de Câncer Gástrico, discute a videolaparoscopia no GIST gástrico, ressaltando sua indicação, as vantagens e os riscos desse procedimento.
 Laercio Gomes Lourenço (foto), chefe do Grupo de Esôfago, Estômago, Duodeno e Intestino Delgado do Departamento de Cirurgia da Universidade Federal de São Paulo (UNIFESP) e presidente da Associação Brasileira de Câncer Gástrico, discute a videolaparoscopia no GIST gástrico, ressaltando sua indicação, as vantagens e os riscos desse procedimento.
Laercio Gomes Lourenço (foto), chefe do Grupo de Esôfago, Estômago, Duodeno e Intestino Delgado do Departamento de Cirurgia da Universidade Federal de São Paulo (UNIFESP) e presidente da Associação Brasileira de Câncer Gástrico, discute a videolaparoscopia no GIST gástrico, ressaltando sua indicação, as vantagens e os riscos desse procedimento.
{jathumbnail off}Introdução
O tumor estromal gastrointestinal (GIST) é uma neoplasia rara, porém, é o segundo tumor mais frequente do aparelho digestivo. O estômago é local mais comumente acometido (70% a 80%) dos casos de GIST. O melhor tratamento é cirúrgico e a videolaparoscopia (cirurgia minimamente invasiva) é hoje uma das principais vias de acesso. A laparotomia aberta clássica também tem seu espaço, não havendo contestação quando os GIST gástricos são maiores de 10 cm de diâmetro.
Desenvolvimento
Os GISTs se originam na camada muscular da parede gastrointestinal podendo assumir formas macroscópicas endofíticas, intramural, exofítica ou mista (Tabela 1). Diante de toda lesão submucosa gástrica deve-se suspeitar de GIST. Dados endoscópicos como tamanho, localização, presença de úlcera devem ser relatados para o diagnóstico e tratamento. A biópsia deve ser realizada sempre que possível em todas as lesões maiores de 1 cm, porém, nem sempre é factível realizar a biópsia, pois pode haver grande dificuldade técnica, principalmente em lesões menores de 1 cm. A patologia está bem definida. Desde 1999, Hirota e col. definiram o padrão imuno-histoquímico com CD 117 (80 a 90 % dos GIST expressam a proteína Kit), marca registrada dos GIST. Outros marcadores incluem o CD34 (30 a 60% de positividade) e DOG (DiscoveronGist) em mais de 85% dos casos.
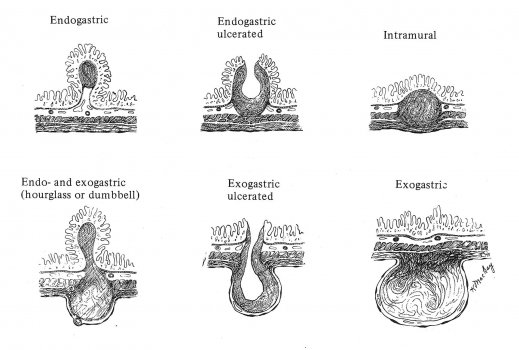
Figura 1 – Formas macroscópicas dos Gist Gástricos.
A maioria dos GIST não causam sintomas, sendo frequentemente achado acidental em exames de endoscopia digestiva alta ou de imagem, como tomografia computadorizada ou ressonância magnética, realizados por outro sintoma ou por checkup. Quando sintomáticos, os GIST podem causar hemorragia digestiva alta de intensidade e repercussão clínica variável. Outro sintoma pode ser de compressão extrínseca de outros órgãos (cólon, estômago, vias biliares) e de massa abdominal palpável.
Lesões maiores de 2 cm ou, para outros autores, maiores de 1 cm devem ser ressecadas para confirmação diagnóstica e avaliação do potencial de malignidade segundo a classificação de Fletcher e Miettenn de 2005, que considera o tamanho, tipo histológico e índice mitótico.
Tratamento Cirúrgico
O tratamento dos GIST é cirúrgico, mas nem todo GIST gástrico deve ser operado. Segundo a NIH (National Institute of Health – USA) GIST menores de 2 cm podem ser observados por endoscopia e/ou imagem a cada 6 ou 12 meses, pois apresentam baixo potencial de malignidade.
A indicação cirúrgica de lesões menores de 1 cm e suspeitas de GIST é ainda controversa. Um numero significante de GIST menores de 2 cm pode ter uma evolução “benigna”. Entretanto, os guidelines da NCCN indicam que GIST menores de 2 cm devem ser periodicamente avaliados por endoscopia e por ecoendoscopia em casos selecionados. A Sociedade Europeia de Oncologia (ESMO) e também o guideline japonês para GIST recomendam ressecção cirúrgica em GIST maiores de 1 cm. Isto deve-se ao estudo realizado por XX que demonstrou que o índice mitótico aumenta dramaticamente nos GIST maiores de 1 cm. GIST maiores de 1,4 cm com margem irregular estavam significantemente com doença em progressão. Os resultados desse estudo sugerem diferentes atividades de proliferação nos GIST entre 1 e 2 cm. Portanto, é compreensível porque alguns serviços recomendam a observação somente em lesões submucosas menores de 1 cm e realizam ressecção em todas as lesões maiores de 1 cm.
A preferência atual para a ressecção dos GIST é a via laparoscópica. As vantagens da laparoscopia são conhecidas, como menor dor no pós-operatório, melhor recuperação e menor tempo de internação.
Os princípios básicos da cirurgia oncológica devem ser respeitados também quando se realiza a cirurgia minimamente invasiva. Tais princípios incluem a manipulação excessiva e rotura tumoral intra-abdominal.
O uso de suturas mecânicas propiciou uma vantagem nessa ressecção, permitindo além da boa hemostasia da parede gástrica uma menor incidência de deiscência da sutura. Uma importante análise da localização permitirá uma cirurgia rápida e segura, sem comprometer a vascularização e/ou inervação da câmara gástrica. GIST localizados no antro devem ser bem avaliados, pois sua ressecção pode comprometer o esvaziamento gástrico e causar estenoses. A ressecção em cunha é a melhor opção, mas em alguns casos a gastrectomia parcial se faz necessária para esvaziamento gástrico adequado. Uma interessante alternativa quando os GIST se localiza em locais estratégicos, como cárdia, antro ou pequena curvatura, é a realização concomitante de endoscopia intra-operatória. Na dúvida, é melhor optar pela gastrectomia e reconstrução a Billroth I ou Y de Roux. A margem de segurança para GIST pode ser milimétrica. Em GIST de muito baixo ou baixo grau, o comprometimento microscópico não parece necessitar de re-intervenção com ampliação, pois nesta condição específica parece não comprometer o prognóstico.
Conclusão
A cirurgia minimamente invasiva no tratamento dos GIST gástrico pode ser realizada em lesões menores de 10 cm, é segura e factível. A curva de aprendizado citada na literatura é de 40 casos de cirurgia gástrica. Porém, raros são os serviços que dispõem dessa casuística.
Autor: Laercio Gomes Lourenço
Professor Associado de Cirurgia da Universidade Federal de São Paulo
Chefe do Grupo de Esôfago, Estômago, Duodeno e Intestino Delgado do Departamento de Cirurgia da UNIFESP.
Presidente da Associação Brasileira de Câncer Gástrico
Coordenador do Grupo de Estudo em GIST e TNE do Hospital Alemão Oswaldo Cruz
Referências:
Submucosal tumors: Comprehensive guide for the diagnosis and therapy of
gastrointestinal submucosal tumors- Nishida T,Kawai N,Yamaguchi S, Nishida Y - Digestive Endoscopy2013; 25: 479–489
Clinical efficacy comparison between laparoscopic and open surgery in the treatment of gastric gastrointestinal stromal tumor- Yan P, Liu J, Hu X, Liu J, Wu Y, Zhao Y, Yu P, Qian F.. Zhonghua Wei Chang Wai Ke Za Zhi. 2015: 25;18(8):808-11








