 Pesquisadores canadenses lançaram o primeiro teste clínico de uma nova terapia experimental que utiliza a combinação de dois vírus para atacar e matar as células cancerosas, e estimular uma resposta imunológica anti-câncer. Pesquisas anteriores sugerem que a abordagem pode ser muito poderosa e ter menos efeitos colaterais do que a quimioterapia convencional e a radioterapia.
Pesquisadores canadenses lançaram o primeiro teste clínico de uma nova terapia experimental que utiliza a combinação de dois vírus para atacar e matar as células cancerosas, e estimular uma resposta imunológica anti-câncer. Pesquisas anteriores sugerem que a abordagem pode ser muito poderosa e ter menos efeitos colaterais do que a quimioterapia convencional e a radioterapia.
A terapia está sendo desenvolvida em conjunto por David Stojdl e John Bell, da Universidade de Ottawa, e Brian Lichty, da Universidade McMaster. Financiado pelo Instituto de Pesquisa do Câncer de Ontário e coordenado pelo NCIC Clinical Trials Group, o estudo espera inscrever até 79 pacientes em quatro hospitais no Canadá. Até 24 pacientes receberão um dos vírus e o restante receberá os dois, com intervalo de duas semanas.
"Descobrimos que quando as células normais se tornam cancerosas, elas adquirem mutações genéticas que lhes permitem crescer muito rapidamente, mas estas mesmas mutações também as tornam mais sensíveis aos vírus", explicou Bell, cientista sênior do Hospital de Ottawa e professor da Universidade de Ottawa.
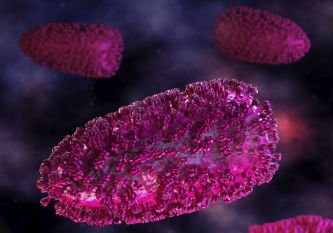
Os dois vírus testados no estudo são chamados MG1MA3 e AdMA3. MG1MA3 (foto) é derivado de um vírus denominado Marabá, que foi isolado pela primeira vez a partir de flebotomíneos brasileiros, enquanto AdMA3 é derivado de um vírus da gripe comum chamado adenovírus. Ambos foram modificados para estimular uma resposta imunológica contra células de câncer que expressam uma proteína chamada MAGE-A3. O vírus Marabá também atinge uma camada extra de atividade anti-câncer por se replicar dentro de muitos tipos de células cancerosas e matá-las diretamente. Os vírus são fabricados em instalações especializadas no Hospital de Ottawa e na Universidade McMaster.
O vírus Maraba é parte de um grande programa canadense de desenvolvimento de estudos clínicos em bioterapia, que é a combinação de vírus e vacinas com terapias convencionais e emergentes para o tratamento de diferentes tipos de tumores. "A ideia por trás desse estudo é usar o adenovírus para preparar o sistema imunológico do paciente a reconhecer a doença e, em seguida, usar o vírus Marabá para matar diretamente o câncer e estimular ainda mais o seu sistema imunológico para evitar a recidiva" disse Brian Lichty, professor associado da Universidade McMaster.
São elegíveis pacientes com mais de 18 anos, de ambos os sexos, com tumor sólido localmente avançado/metastático confirmado histologicamente, irressecável, com expressão positiva de MAGE-A3 (lesão primária ou metastática) e para o qual não há terapia padrão conhecida que prolongue a sobrevida.
A fase I do estudo busca encontrar a dose indicada da nova terapia, seja com o vírus MG1 Marabá/MAGE-A3 (MG1MA3) administrado isoladamente ou em combinação com o adenovírus/MAGE-A3 (AdMA3). Os participantes receberão uma ou as duas terapias e serão acompanhados para verificar os efeitos adversos. Se forem graves em relação aos pacientes com o primeiro nível de dose, a dose de MG1MA3 pode ser reduzida. Se os efeitos adversos não forem graves, os participantes receberão doses mais elevadas, até que o maior nível de dose possível seja alcançado.
Além do Hospital de Ottawa, participam do ensaio clínico o Juravinski Cancer Centre of Hamilton Health Sciences, Princess Margaret Cancer Centre daUniversity Health Network, em Toronto, e o Vancouver Centre of the BC Cancer Agency.
O estudo foi aprovado pela Health Canada, Ontario Cancer Research Ethics Board e BC Cancer Agency Research Ethics Board.
Referência: A Phase I/II Study of MG1 Maraba/MAGE-A3 (MG1MA3), With and Without Adenovirus Vaccine, With Transgenic MAGE-A3 Insertion (AdMA3) in Patients With Incurable Advanced/Metastatic MAGE-A3-Expressing Solid Tumours








