 Dez anos depois de lançar o projeto piloto de notificação eletrônica em São Paulo, a vigilância sanitária reconhece que é preciso vencer o desafio da subnotificação e confirma que a participação da oncologia se mantém tímida. A vigilância sanitária diz que notificar uma reação adversa é um processo simples, rápido e seguro.
Dez anos depois de lançar o projeto piloto de notificação eletrônica em São Paulo, a vigilância sanitária reconhece que é preciso vencer o desafio da subnotificação e confirma que a participação da oncologia se mantém tímida. A vigilância sanitária diz que notificar uma reação adversa é um processo simples, rápido e seguro.
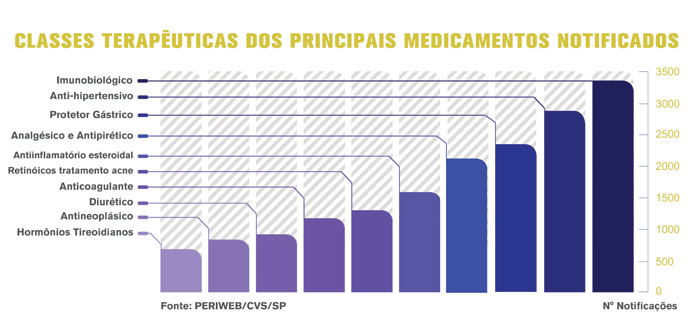 Quando notifica um evento adverso associado ao uso de diferentes tecnologias sanitárias, médicos e outros profissionais de saúde contribuem para reforçar os serviços de farmacovigilância. Mas a realidade prática mostra que precisamos avançar. Em São Paulo, a base de dados do Programa Estadual de Farmacovigilância (PERIWEB) somou 150 mil notificações em dez anos, com a média mensal de 2 mil registros. Desse total, 92% são notificações de eventos adversos e associados à qualidade de medicamentos, mas os números consolidados também mostram a tímida participação da oncologia e revelam alta frequência de notificações que não trazem sequer informação sobre a idade ou o sexo do paciente.
Quando notifica um evento adverso associado ao uso de diferentes tecnologias sanitárias, médicos e outros profissionais de saúde contribuem para reforçar os serviços de farmacovigilância. Mas a realidade prática mostra que precisamos avançar. Em São Paulo, a base de dados do Programa Estadual de Farmacovigilância (PERIWEB) somou 150 mil notificações em dez anos, com a média mensal de 2 mil registros. Desse total, 92% são notificações de eventos adversos e associados à qualidade de medicamentos, mas os números consolidados também mostram a tímida participação da oncologia e revelam alta frequência de notificações que não trazem sequer informação sobre a idade ou o sexo do paciente.
“Foi o primeiro sistema eletrônico no Brasil para notificação de reações adversas. De positivo, acumulamos a experiência de alertas sanitários e boletins informativos, com ações que em alguns casos culminaram na retirada de medicamentos do mercado, como aconteceu em 2008 com o antiinflamatório Prexige®, e com o alerta de 2014 contra algumas incretinas utilizadas off-lable em regimes de emagrecimento, ignorando o risco de câncer pancreático e de tireoide”, conta Adalton Guimarães Ribeiro, diretor de farmacovigilância do Centro de Vigilância Sanitária (CVS) de São Paulo.
Há muito tempo a ciência já demonstrou que a mesma substância que cura também tem o potencial de matar. Essa dualidade, que ganhou expressão com a tragédia da talidomida, faz da farmacovigilância uma atividade indispensável, com o objetivo de reduzir as taxas de morbi-mortalidade associadas ao uso de medicamentos. No caso de uma doença grave, como o câncer, em que drogas complexas e muitas vezes inovadoras fazem parte do arsenal de tratamento, a farmacovigilância assume uma dimensão ainda mais importante e cumpre papel estratégico no monitoramento da qualidade, eficácia e segurança terapêutica.
Reconhecer que a toxicidade pode ser um fator limitante primário no tratamento do câncer é um incentivo a mais para fomentar a farmacovigilância oncológica, que sem dúvida precisa ganhar escala. “Ainda não está completamente disseminada a cultura da notificação espontânea, principalmente na oncologia, onde a ocorrência de um efeito adverso passa muitas vezes como um evento esperado”, explica o diretor do CVS de São Paulo.
Outro equívoco é considerar que apenas as reações adversas precisam ser notificadas. Qualquer desvio da qualidade, assim como a suspeita de perda de eficácia de um agente terapêutico, também precisam ser notificados, mas a julgar pelos números do CVS configuram situações de exceção. A maioria esmagadora das notificações, 92%, está relacionada à suspeita de reações adversas e 8% correspondem a notificações de desvios de qualidade.
“As ações de farmacovigilância de muitas instituições hospitalares ainda são incipientes e diminuem a confiabilidade das informações registradas”, critica Ribeiro. Por essas e outras, é a própria indústria farmacêutica, por exigência legal, que lidera a base de dados do CVS, com 77% do total de notificações.
Nos imunobiológicos, reações com agentes como rituximabe foram mais notificadas pelas equipes envolvidas no tratamento das doenças autoimunes do que pela oncologia, embora sejam agentes amplamente empregados também no tratamento do câncer.
Prontuário
A Portaria 529 de 2013, que instituiu o Programa Nacional de Segurança do Paciente, prevê que todo hospital tenha um núcleo de segurança do paciente, que em tese recebe as notificações de reações adversas. O problema é que para notificar é preciso ter informações consistentes, o que significa ter um prontuário com dados capazes de subsidiar essas interfaces de cuidado. O CVS avisa que não adianta bater na tecla da notificação sem ter informação adequada para gerar registros confiáveis e se queixa de que os hospitais reportam aquilo que é visível- náusea, vômito, diarréia, rush cutâneo - e muitas vezes se esquecem de notificar outras reações, que nem sempre são monitoradas no ambiente clínico.
Em síntese, não é difícil notificar, mas a verdade é que dá trabalho reunir e estruturar as informações, um alerta de que vale à pena dedicar atenção aos dados do prontuário do paciente.
Outra recomendação é constituir uma comissão de farmacovigilância. Assim, qualquer profissional que suspeitar de reação adversa tem condição de acionar um membro da comissão e efetivar a notificação. Com a participação de um médico, um profissional de enfermagem e um farmacêutico, por exemplo, já é possível avançar na farmacovigilância.
Perfil de segurança
Em agentes de uso intravenoso ou intratecal são comuns as reações infusionais, mas algumas realmente despertam atenção. “Houve um hospital que comprou um oncológico mais barato, mas o tempo de infusão desse medicamento era maior. No entanto, diante da quantidade de pacientes no fluxo de atendimento, eles mantiveram o menor tempo infusional e, evidentemente, muitos pacientes apresentaram reação”, ilustrou o CVS.
E não são apenas os ‘velhos‘ citotóxicos que devem figurar nos programas de vigilância. As drogas de última geração também são tóxicas e merecem atenção redobrada. “Em novos medicamentos o olhar precisa ser ainda mais cauteloso”, ensina o diretor do CVS, que atuou como consultor da Unesco em programas de farmacovigilância. Principalmente nos primeiros anos de comercialização, a farmacovigilância auxilia na identificação de reações adversas desconhecidas, que muitas vezes não aparecem no ambiente dos ensaios clínicos. “É uma molécula nova, requer uma vigilância intensa. Grande parte dos medicamentos que historicamente já foram retirados do mercado por problemas com o perfil de segurança foram reavaliados nessa fase, nos primeiros cinco anos pós-comercialização”, diz o especialista.
A mesma regra vale para agentes terapêuticos que perderam a proteção patentária e tiveram a produção made in Brazil, com a chancela do Ministério da Saúde. Na prática da oncologia, se o paciente trocou de medicamento, fica claro que só é possível identificar possíveis problemas se isso for monitorado, para saber se o switch tem a mesma qualidade e se é tão seguro e eficaz como o de referência.
A relação médico-paciente é um contexto único e diante da simples suspeita na relação risco/benefício, a própria Sociedade Brasileira de Oncologia Clínica (SBOC) recomenda que os oncologistas sejam mais proativos. A própria SBOC deve anunciar em breve uma plataforma eletrônica para a notificação de reações adversas, com apoio da SOBRAFO, a Sociedade Brasileira de Farmacêuticos em Oncologia.
Como notificar
 Annemeri Livinalli (foto), da SOBRAFO, reforça a importância da farmacovigilância oncológica e lembra aos profissionais da saúde a necessidade de reduzir cada vez mais asubnotificação de reações adversas a medicamentos. Confira a seguir algumas recomendações:
Annemeri Livinalli (foto), da SOBRAFO, reforça a importância da farmacovigilância oncológica e lembra aos profissionais da saúde a necessidade de reduzir cada vez mais asubnotificação de reações adversas a medicamentos. Confira a seguir algumas recomendações:
Quais são os pilares de uma correta notificação de reações adversas a medicamentos e a quem cabe notificar?
As notificações podem ser feitas por qualquer profissional da área de saúde e de forma espontânea. Os pilares para o sucesso do processo da farmacovigilância que se inicia com a notificação são a busca ativa, a sensibilização e a capacitação de todos os profissionais que voluntariamente devem relatar à vigilância sanitária as reações adversas nos pacientes e os desvios de qualidade observados nos medicamentos.
O que reportar?
Em 2011, a SOBRAFO publicou em parceria com a ANVISA a segunda edição do Guia para notificação de reações adversas em oncologia, pois uma dúvida constante dos profissionais era exatamente essa: “o que notificar?” Como os medicamentos antineoplásicos causam com frequência diversas reações adversas, há necessidade de estabelecer critérios para notificar o que realmente é necessário e representa impacto na farmacovigilância. Assim, recomendamos notificar qualquer reação adversa que não esteja descrita em bula ou na literatura; qualquer reação graus 3 e 4 (conforme descrito no CTCAE) causada por medicamentos comercializados há mais de 5 anos, mesmo os descritos em bula; e para os medicamentos com menos de 5 anos de comercialização, relatar a reação de qualquer grau, mesmo que descrita em bula ou na literatura.
E uma situação de inefetividade terapêutica, também pode ser notificada?
A inefetividade, embora também possa ser notificada, é uma situação particular e que desperta insegurança nos profissionais, pois diversos fatores podem interferir no efeito do medicamento, entre eles a resistência tumoral. Já o desvio de qualidade, esse sim deve sempre ser notificado e infelizmente é pouco relatado no Brasil.
Com a chegada dos medicamentos biossimilares na oncologia, crescem os desafios da farmacovigilância. Como podemos nos preparar desde já para esse novo cenário?
Primeiro, é necessário compreender o que são esses medicamentos, como ocorre a produção, pois somente assim os profissionais da saúde vão compreender que não se trata de uma produção convencional, que muitos desses medicamentos biológicos passam por um processo fabril de difícil replicação e que as análises de controle de qualidade podem variar entre os laboratórios fabricantes. Tendo bem esclarecido que são medicamentos de difícil padronização entre lotes e entre fabricantes, impreterivelmente faz-se necessário uma vigilância mais constante. Um grande auxílio para os serviços de oncologia é a criação de uma área específica para a farmacovigilância, com infraestrutura e profissional preparado para realizar a busca ativa, educar os envolvidos, notificar e acompanhar os desfechos.
Que recomendações a SOBRAFO pode fazer aos centros de câncer interessados em aprimorar suas práticas de farmacovigilância?
Primeiramente, que estabeleçam as rotinas de farmacovigilância, designando um profissional para se responsabilizar por essa área. Os serviços que já fizeram essa experiência tiveram um aumento considerável de relatos de reação adversa. Inevitavelmente, isso se reflete na qualidade do cuidado prestado ao paciente, gera mais conforto aos profissionais e resulta em dados de extrema importância para as vigilâncias sanitárias, em nível estadual ou federal. No fim, tudo se reflete em segurança para o paciente, que é um dos principais objetivos do tratamento, eliminar ou controlar a doença, com segurança.








