O Novembro Azul, campanha realizada pela Sociedade Brasileira de Urologia (SBU) e pelo Instituto Lado a Lado pela Vida, busca conscientizar a população masculina sobre a importância de cuidar melhor da sua saúde.Não é para menos. Um estudo realizado pela SBU mostrou que 51% dos homens nunca consultaram um urologista.
O Novembro Azul, campanha realizada pela Sociedade Brasileira de Urologia (SBU) e pelo Instituto Lado a Lado pela Vida, busca conscientizar a população masculina sobre a importância de cuidar melhor da sua saúde.Não é para menos. Um estudo realizado pela SBU mostrou que 51% dos homens nunca consultaram um urologista.
O estudo, realizado no mês de julho em parceria com a Bayer, contou com a participação de 3.200 homens com mais de 35 anos, em oito cidades brasileiras (São Paulo, Rio de Janeiro, Brasília, Porto Alegre, Belo Horizonte, Salvador, Recife e Curitiba).
Doença mais prevalente nos homens, o câncer de próstata tem estimativa de 69 mil novos casos1 ao ano. O diagnóstico precoce é essencial para o tratamento. Quando descoberto no início, as chances de cura do câncer de próstata chegam a 90%.
Pessoas da raça negra e com familiares de primeiro grau que tiveram a doença devem procurar um urologista para avaliar a necessidade de iniciar seus exames a partir dos 45 anos. O exame da próstata consiste no toque retal e na dosagem sérica do PSA no sangue. A realização de exames nessa faixa etária está relacionada à diminuição de cerca de 21% na mortalidade pela doença.
Na maioria dos casos iniciais, o paciente não tem sintomas e só a avaliação rotineira com o exame de PSA e o toque retal permitem estabelecer a suspeita e prosseguir na investigação. Nos casos classificados como de baixo risco é indicada a vigilância ativa, baseada na observação da evolução do quadro sem intervenções terapêuticas.
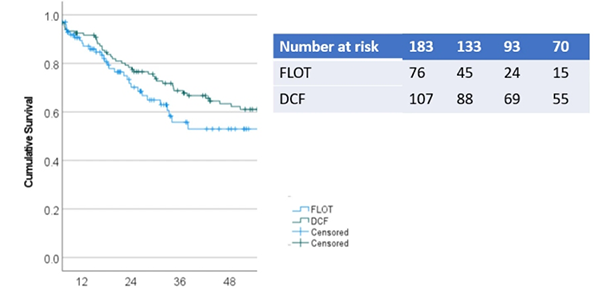
Para os casos em estadio avançado, medicamentos podem proporcionar sobrevida e uma melhor qualidade de vida ao paciente, retardando a progressão do tumor.
Novembro Azul
Ao longo do mês serão realizadas ações em todos os Estados brasileiros, que contemplam a iluminação de pontos turísticos e monumentos, palestras informativas para leigos, intervenções em locais de grande circulação, além do VIII Fórum de Políticas Públicas e Saúde do Homem, que será realizado no dia 17 de novembro – Dia Nacional de Combate ao Câncer de Próstata – na Câmara dos Deputados, em Brasília.
Referência: 1 - Estimativas para o câncer de próstata 2014 do Instituto Nacional do Câncer (Inca)