Todo gene, que contém éxons e íntrons, é transcrito em uma longa molécula de RNA (pré-RNAm), também dotada de éxons e íntrons. Em seguida, ocorre remoção dos íntrons, o que reduz o tamanho do RNA inicial. Finalmente os éxons se ligam, formando o RNAm funcional ou maduro, que, contendo apenas segmentos codificadores (éxons), migra para o citoplasma, onde vai ser traduzido em cadeia polipetítidica. Esse processamento do RNA é chamado de splicing (que ocorre no núcleo e consiste na remoção dos íntrons e união dos éxons imediatamente após a transcrição do RNA) e é bastante complexo, já que a molécula de RNA deve ser clivada em locais exatos e os éxons devem ser unidos também de maneira correta.
Os íntrons retirados do pré-RNA são “destruídos” dentro do núcleo gerando nucleotídeos livres, que por sua vez são reciclados.
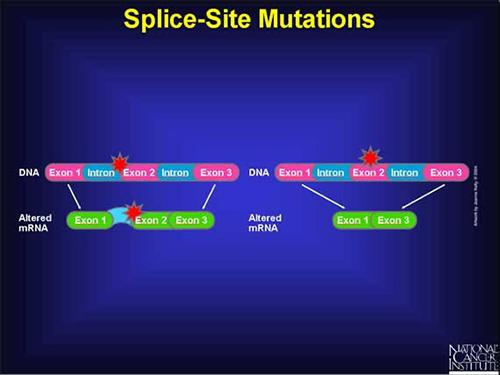
Mutações em sítios splicing:
O splicing requer uma extrema precisão das moléculas envolvidas no processo, já que o acréscimo ou a remoção de um único nucleotídeo em um éxon pode alterar a fase de leitura e produzir uma proteína bastante diferente da original, caracterizando uma mutação, decorrente portanto, de erros no splicing. Estima-se atualmente que erros ou mutações no processo de splicing causem cerca de 10% das doenças genéticas.
Mutações splicing do Exon 14 do gene MET:
O receptor do fator de crescimento de hepatócitos (do inglês hepatocyte growth factor receptor ou HGFR) é um receptor com atividade tirosina quinase codificado pelo gene MET e tem papel fundamental no desenvolvimento embrionário pulmonar. Este alvo ganhou importância com a descoberta recente de mutações em sítios de splicing em adenocarcinomas pulmonares. Estas mutações levam à perda da codificação do exon 14 e previnem o receptor de se ligar a enzimas com atividade E3 ligase e, por conseguinte, bloqueia a sua degradação. As mutações de perda do exon 14 de MET acontecem em aproximadamente 4% dos adenocarcinomas pulmonares e têm sido testadas como biomarcador de sensibilidade aos inibidores de HGFR, como crizotinibe e, mais recentemente, o capmatinibe, que recebeu do FDA americano um “Breakthrough Therapy Designation” devido aos resultados auspiciosos obtidos pela droga no estudo GEOMETRY.
André Murad MD, PhD, Pós-Doutor em Genética








