Com acompanhamento de 3 anos, a monoterapia com o anticorpo anti-PD-1 cemiplimabe (Libtayo®, Sanofi) continua a demonstrar benefício sustentado de sobrevida global e sobrevida livre de progressão em pacientes com câncer de pulmão de células não pequenas avançado e/ou metastático. A atualização de longo prazo1 do estudo de Fase 3 EMPOWER-Lung 1 apresentada em Sessão Oral no ESMO 2022 também trouxe os dados de sobrevida global e taxa de resposta dos pacientes que progrediram à imunoterapia e continuaram o tratamento com cemiplimabe associado à quimioterapia. “Pela primeira vez, um estudo de Fase 3 demonstra vantagens terapêuticas da manutenção da imunoterapia para pacientes que progridem após a monoterapia em primeira linha com anti-PD-1”, destacam os autores.
O EMPOWER-Lung 1 é um estudo aberto, Fase 3, que incluiu 712 pacientes com câncer de pulmão de células não pequenas (CPCNP) sem tratamento prévio recrutados em 138 centros, de 24 países. Foram elegíveis pacientes adultos (≥18 anos) com doença avançada ou metastática, confirmada histologicamente ou citologicamente, e com bom performance status (ECOG de 0-1). Os pacientes foram randomizados para receber cemiplimabe (350 mg a cada 3 semanas por 108 semanas ou até a progressão da doença; n=357) ou quimioterapia à escolha do investigador (4 a 6 ciclos; n=355). As características do baseline foram bem equilibradas entre os braços de tratamento.
Com acompanhamento de 3 anos, a monoterapia com o anticorpo anti-PD-1 cemiplimabe (Libtayo®, Sanofi) continua a demonstrar benefício sustentado de sobrevida global e sobrevida livre de progressão em pacientes com câncer de pulmão de células não pequenas avançado e/ou metastático. A atualização de longo prazo1 do estudo de Fase 3 EMPOWER-Lung 1 apresentada em Sessão Oral no ESMO 2022 também trouxe os dados de sobrevida global e taxa de resposta dos pacientes que progrediram à imunoterapia e continuaram o tratamento com cemiplimabe associado à quimioterapia. “Pela primeira vez, um estudo de Fase 3 demonstra vantagens terapêuticas da manutenção da imunoterapia para pacientes que progridem após a monoterapia em primeira linha com anti-PD-1”, destacam os autores.
O EMPOWER-Lung 1 é um estudo aberto, Fase 3, que incluiu 712 pacientes com câncer de pulmão de células não pequenas (CPCNP) sem tratamento prévio recrutados em 138 centros, de 24 países. Foram elegíveis pacientes adultos (≥18 anos) com doença avançada ou metastática, confirmada histologicamente ou citologicamente, e com bom performance status (ECOG de 0-1). Os pacientes foram randomizados para receber cemiplimabe (350 mg a cada 3 semanas por 108 semanas ou até a progressão da doença; n=357) ou quimioterapia à escolha do investigador (4 a 6 ciclos; n=355). As características do baseline foram bem equilibradas entre os braços de tratamento.
Os desfechos primários foram sobrevida global e sobrevida livre de progressão (RECIST v 1.1) avaliados por comitê de revisão independente em pacientes com alta expressão de PD-L1 (≥50% das células tumorais).
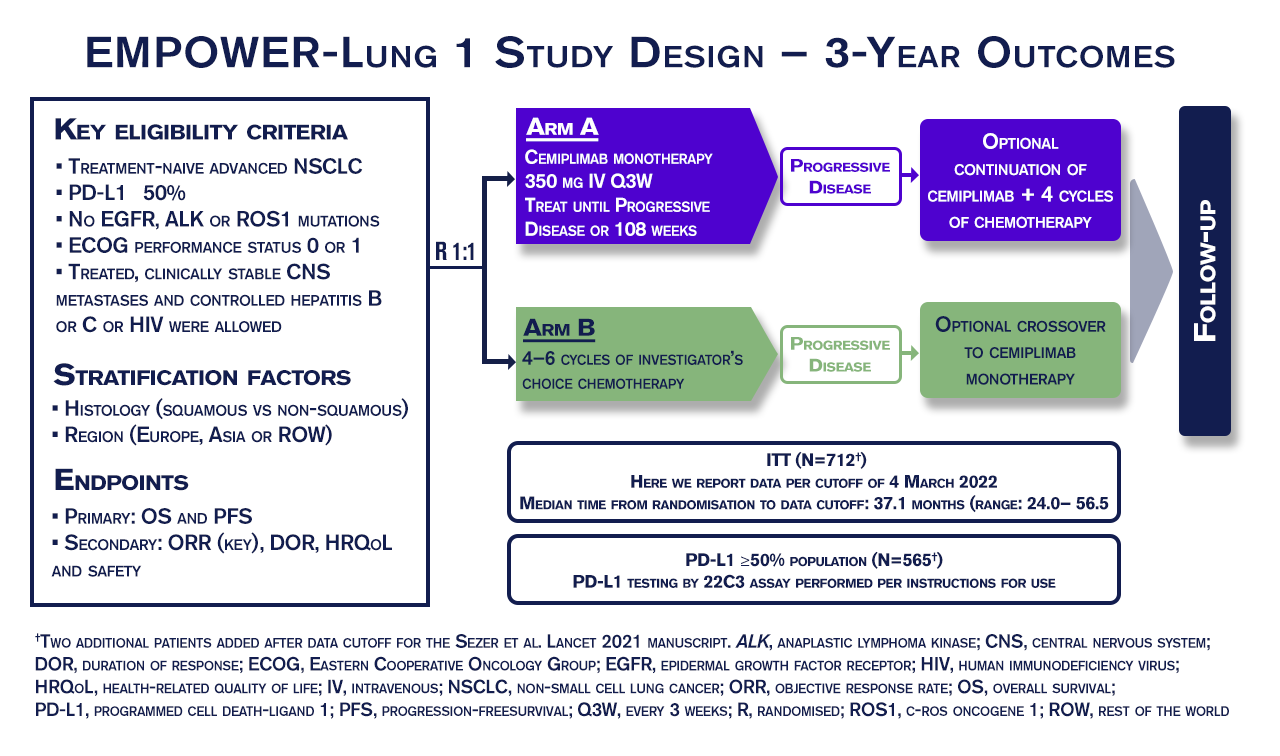
Reportados por Sezer et al. no Lancet Oncology em 20212, os resultados iniciais do estudo demonstraram que cemiplimabe atingiu os principais desfechos de eficácia e segurança, com sobrevida global superior e benefício significativo de sobrevida livre de progressão, embasando a aprovação do tratamento pelas principais agências reguladoras, incluindo a Agência Nacional de Vigilância Sanitária (Anvisa)3. Agora, no ESMO 2022, foram apresentados os dados do seguimento de 3 anos, além de resultados dos pacientes do braço de monoterapia com cemiplimabe que receberam o anti-PD-1 associado a quimioterapia após a progressão da doença.
Resultados de longo prazo em pacientes com expressão de PD-L1 ≥50%
Os resultados do seguimento de longo prazo (mediana de 37,1 meses; intervalo: 24,0-56,5) corroboram o benefício de cemiplimabe em pacientes com câncer de pulmão de células não pequenas avançado e/ou metastático, especialmente na população com alta expressão de PD-L1. No subgrupo de pacientes com expressão de PD-L1 ≥50% (cemiplimabe, n=284; quimioterapia, n=281), cemiplimabe foi associado a melhores resultados. A ORR foi de 46,5% no braço de cemiplimabe e 21% no braço de quimioterapia (OR, 3,264; 95% CI, 2,255-4,724; P <0,0001). As taxas de resposta completa foram de 8,1% e 2,1%, respectivamente.
Neste subgrupo PD-L1-alto, a mediana de sobrevida global foi de 26,1 meses no braço de cemiplimabe e 13,3 meses no braço de quimioterapia (HR, 0,57; 95% CI, 0,46-0,71; P = 0,0001). A mediana de sobrevida livre de progressão foi de 8,1 meses e 5,3 meses, respectivamente (HR, 0,51; 95% CI, 0,42-0,62; P = 0,0001).
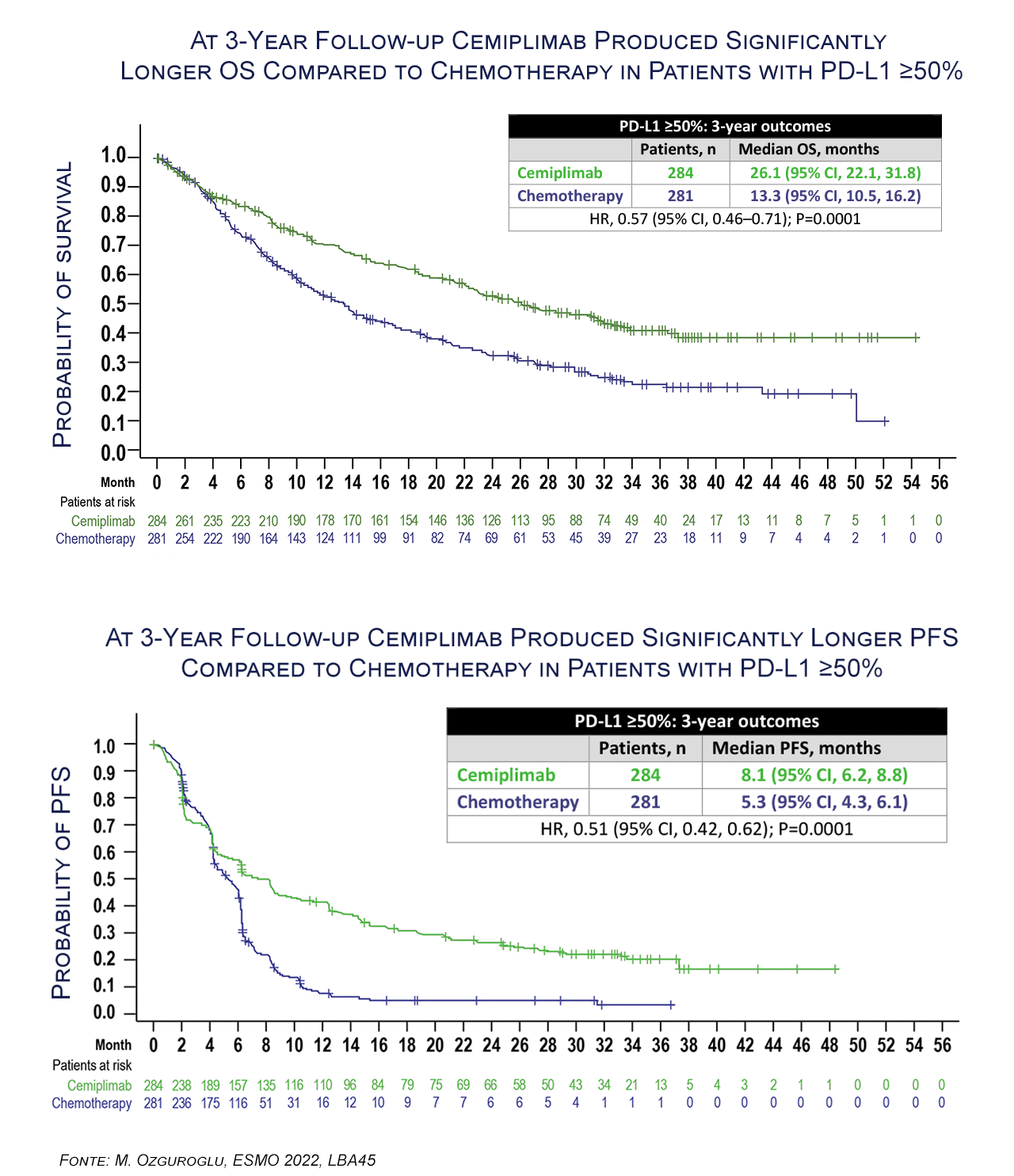
“Os resultados do EMPOWER-Lung 1 mostram que a imunoterapia tem um papel no câncer de pulmão metastático, e que existe um subgrupo de pacientes que se beneficia mais, justamente a população com alta expressão de PD-L1. Esses dados nos deixam seguros de que essa estratégia é eficaz e a imunoterapia isolada pode ser utilizada para a maior parte dos pacientes com alta expressão de PD-L1, reservando a combinação de quimioterapia e imunoterapia para aqueles com expressão mais baixa de PD-L1”, avalia Vladmir Cordeiro de Lima, oncologista do A.C. Camargo Cancer Center.
Segunda linha
Pacientes randomizados para cemiplimabe com progressão de doença confirmada por um comitê de revisão independente e cego (BIRC) foram autorizados a continuar o tratamento com cemiplimabe com adição de até 4 ciclos de quimioterapia. Para inclusão na análise pós-progressão, os pacientes deviam ter recebido pelo menos uma dose anterior de quimioterapia e terem realizado exame de imagem após a progressão ao cemiplimabe. A resposta à continuação de cemiplimabe + quimioterapia foi avaliada por BIRC considerando um novo baseline, definido como a última triagem antes da dose inicial de quimioterapia.
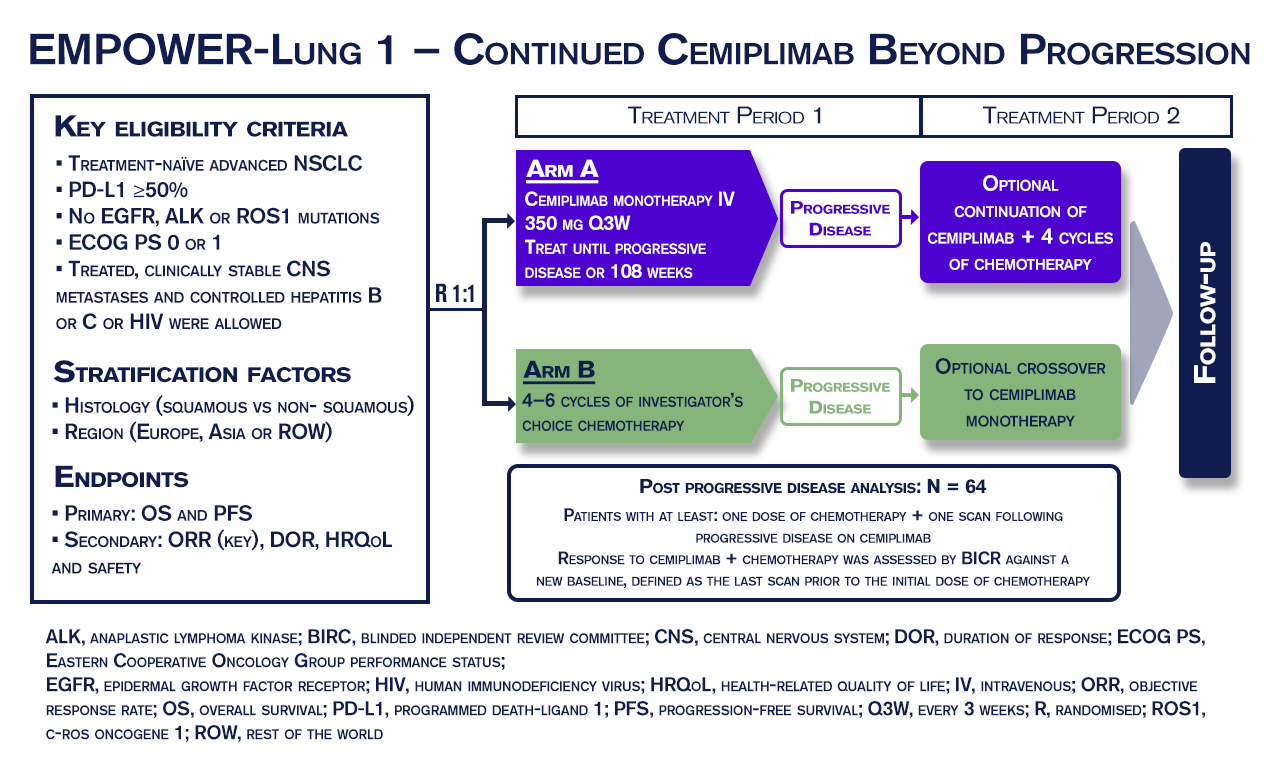
A análise de 64 pacientes do braço de cemiplimabe que apresentaram progressão da doença e permaneceram no tratamento com o anticorpo anti-PD1 associado à quimioterapia demonstrou uma taxa de resposta objetiva de 31,3%, com 3 pacientes atingindo resposta completa. A mediana de sobrevida global (mOS) foi de 15,1 meses (11,3, 18,7).
No geral, o tratamento de segunda linha foi bem tolerado, com 19 pacientes (29,7%) experimentando um evento adverso grave relacionado ao tratamento (TEAE), e descontinuação do tratamento do estudo ou morte em 3 pacientes. “Esse é um dado interessante quando analisamos um seguimento maior, e os resultados indicam que a imunoterapia utilizada por mais tempo não adicionou novas toxicidades, com menos de 5% dos pacientes descontinuando o tratamento por conta de eventos adversos”, observa o oncologista Guilherme Harada, advanced clinical fellow no Memorial Sloan Kettering Cancer Center.
Em síntese, os resultados apresentados no congresso europeu mostram que com seguimento de 3 anos, cemiplimabe continua a proporcionar melhora sustentada na sobrevida livre de progressão e sobrevida global em comparação com quimioterapia, corroborando os dados da análise anterior. “Esse é um achado excepcional no cenário do câncer de pulmão de células não pequenas. Esses resultados apoiam o uso de cemiplimabe como uma opção de tratamento de primeira linha sem quimioterapia para CPCNP avançado e alta expressão de PD-L1.”, concluem os autores.
O estudo foi financiado pela Regeneron Pharmaceuticals, Inc., e Sanofi, e está registrado em ClinicalTrials.Gov; NCT03088540.
Assista vídeo sobre o mesmo assunto:
EMPOWER-Lung 1: resultados de longo prazo no câncer de pulmão de células não pequenas avançado
Os oncologistas Guilherme Harada e Vladmir Lima discutem alguns dos estudos do panorama de câncer de pulmão que concentraram as atenções no congresso europeu. Entre os destaques estão os dados de eficácia com 3 anos de seguimento do estudo EMPOWER-Lung 1, que corroboram os resultados positivos de cemiplimabe em monoterapia versus quimioterapia em pacientes com câncer de pulmão de células não pequenas e expressão de PD-L1 > 50%. Confira, na TV ONCONEWS.
Referências:
1 - Özgüroğlu M, Kilickap S, Sezer A, et al. Three years survival outcome and continued cemiplimab (CEMI) beyond progression with the addition of chemotherapy (chemo) for patients (pts) with advanced non-small cell lung cancer (NSCLC): The EMPOWER-Lung 1 trial. Presented at ESMO 2022; September 9-13, 2022. Abstract LBA54.
https://oncologypro.esmo.org/meeting-resources/esmo-congress/three-years-survival-outcome-and-continued-cemiplimab-cemi-beyond-progression-with-the-addition-of-chemotherapy-chemo-for-patients-pts-with-a
2 - Sezer A, Kilickap S, Gumus M, Bondarenko I, Ozguroglu M, Gogishvili M, et al. Cemiplimab monotherapy for first-line treatment of advanced non-small-cell lung cancer with PD-L1 of at least 50%: a multicentre, open-label, global, phase 3, randomised, controlled trial. Lancet. 2021;397(10274):592-604
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(21)00228-2/fulltext
3 - Diário Oficial da União - Resolução-RE nº 1.650, de 19 de maio de 2022 - Publicado em: 23/05/2022 | Edição: 96 | Seção: 1 | Página: 258
https://www.in.gov.br/en/web/dou/-/resolucao-re-n-1.650-de-19-de-maio-de-2022-401806579
--