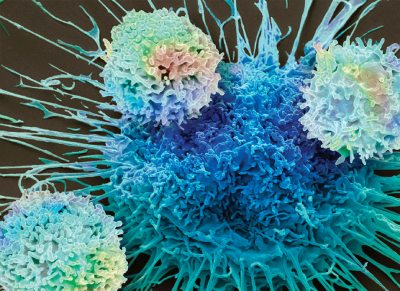
 A terapia com células T do receptor de antígeno quimérico (CAR) trouxe impacto sem precedentes no tratamento de malignidades hematológicas, como leucemia linfoblástica aguda, linfoma de células B e mieloma múltiplo, mas a eficácia das CAR T cells em tumores sólidos permanece limitada. Dois estudos publicados na Nature trazem novos insights que podem melhorar a eficácia das CAR T cells contra tumores sólidos.
A terapia com células T do receptor de antígeno quimérico (CAR) trouxe impacto sem precedentes no tratamento de malignidades hematológicas, como leucemia linfoblástica aguda, linfoma de células B e mieloma múltiplo, mas a eficácia das CAR T cells em tumores sólidos permanece limitada. Dois estudos publicados na Nature trazem novos insights que podem melhorar a eficácia das CAR T cells contra tumores sólidos.
No microambiente do tumor sólido, as CAR T cells estão predispostas a se diferenciarem em resposta à estimulação crônica do antígeno, à competição metabólica e à falta de sinais co-estimulatórios apropriados. Uma abordagem de engenharia genética mostrou com sucesso como preservar as células tronco das CAR T cells, mantendo sua eficácia e aptidão metabólica.
“Mostramos que a superexpressão de FOXO1 promove um fenótipo semelhante a um ´tronco´ em CAR T cells derivadas de doadores humanos saudáveis ou de pacientes, o que se correlaciona com melhor aptidão mitocondrial, persistência e eficácia terapêutica in vivo. Este trabalho revela, assim, uma abordagem de engenharia para reforçar geneticamente um fenótipo metabólico favorável que tem alto potencial translacional para melhorar a eficácia das CAR T cells contra tumores sólidos”, descreve análise de Phillip K. Darcy e colegas.
Os pesquisadores procuraram identificar os principais fatores de transcrição que são regulados positivamente pela IL-15, uma vez que a IL-15 aumenta a persistência e o metabolismo das CAR T cells. A análise do epigenoma e do transcriptoma das células CAR T cultivadas na presença de IL-15 revelou forte enriquecimento da assinatura do gene FOXO1. “A superexpressão de uma variante constitutivamente ativa de FOXO1 (FOXO1-ADA) em CAR T cells específicas de HER2 de camundongo ou FOXO1 de tipo selvagem em CAR T cells humanas (Lewis Y CAR T cells) melhorou a aptidão metabólica, levando em última análise a um controle aprimorado de tumores sólidos”, destaca o artigo de Chan et al. “Notavelmente, a superexpressão de FOXO1 manteve o 'tronco' das células CAR T e aumentou a persistência em maior extensão do que outros reguladores transcricionais regulados positivamente pela IL-15”, esclarecem.
Outro grupo de pesquisadores, liderado por Evan W. Weber, da Universidade da Pennsylvania, e pela imunologista Crystal Mackall, da Universidade de Stanford, também se concentrou no fator de transcrição FOXO1, agora identificado como um regulador mestre da programação de memória em células CAR T.
Uma limitação importante das terapias com CAR T cells é a fraca persistência dessas células in vivo”, explicam Weber e colegas, que se concentraram em desvendar caminhos capazes de preservar a memória nas células CAR T, fortalecendo sua persistência a longo prazo e, consequentemente, sua eficácia clínica. “Mostramos que o fator de transcrição FOXO1 é responsável por promover a memória e restringir a exaustão em células CAR T humanas. A inibição farmacológica ou edição genética do FOXO1 endógeno diminuiu a expressão de genes associados à memória, promoveu um fenótipo semelhante à exaustão e prejudicou a atividade antitumoral das células CAR T”, descrevem. Por outro lado, as células CAR T que superexpressaram FOXO1 mantiveram sua função, potencial de memória e aptidão metabólica em ambientes de estimulação crônica, assim como exibiram maior persistência e controle tumoral in vivo.
As pesquisas de Weber e colegas ressaltam a relevância clínica do FOXO1 na imunoterapia contra o câncer. “Nossos resultados mostram que a superexpressão de FOXO1 pode aumentar a atividade antitumoral das CAR T cells humanas e destacam a reprogramação da memória como uma abordagem amplamente aplicável para otimizar os estados terapêuticos das células T”.
Referências:
Chan, J.D., Scheffler, C.M., Munoz, I. et al. FOXO1 enhances CAR T cell stemness, metabolic fitness and efficacy. Nature (2024). https://doi.org/10.1038/s41586-024-07242-1
Doan, A.E., Mueller, K.P., Chen, A.Y. et al. FOXO1 is a master regulator of memory programming in CAR T cells. Nature (2024). https://doi.org/10.1038/s41586-024-07300-8